ExoSwitch – biopsie liquide pour le diagnostic précoce du cancer
Cancer : un diagnostic peu performant
Le cancer est l’une des principales causes de décès dans le monde. Un cancer apparaît lorsque des cellules saines acquièrent de nouvelles propriétés à la suite de l’accumulation de mutations, ce qui entraîne la croissance de la tumeur. Ainsi, il est désormais largement admis que le cancer est une “maladie du génome”. La procédure classique de diagnostic est une biopsie d’un échantillon de tissu tumoral : elle permet aux cliniciens d’analyser de près la tumeur suspectée. Cependant, cette méthode présente de nombreux inconvénients.
La biopsie est une procédure invasive et souvent douloureuse, et le prélèvement de tissu peut être impossible pour les organes difficilement accessibles (ex: le cerveau). De plus, la biopsie conventionnelle nécessite de connaître la localisation de la tumeur. Or, au cours des premiers stades de développement, la maladie est asymptomatique. De ce fait, la plupart des découvertes de tumeurs à des stades précoces sont accidentelles et rares. Enfin, les biomarqueurs tumoraux (molécules biologiques quantifiables indiquant la présence/ progression d’un cancer) les plus fiables détectés lors d’une biopsie n’apparaissent souvent qu’à des stades avancés, ce qui contribue à un diagnostic tardif. Le dépistage tardif de la maladie est une limitation majeure pour la mise en place de traitement, notamment pour les cancers les plus agressifs qui sont associés à une durée de vie réduite et à une mortalité élevée.
Comment détecter un cancer plus tôt ?
La détection précoce du cancer est associée à une amélioration de la survie, offrant ainsi une voie prometteuse pour réduire le taux de mortalité due au cancer. L’une des pistes prometteuses est le prélèvement d’échantillons de fluides biologiques (sang, urine, salive…) chez le patient. Une tumeur, même à un stade précoce, interagit avec le reste de l’organisme en sécrétant des molécules de signalisation (protéines et des acides nucléiques) dans le sang, l’urée, la salive, etc. La découverte de ces biomarqueurs a conduit au développement de nouvelles approches comme la biopsie liquide -non invasive, précise et rapide pour détecter les biomarqueurs associés au cancer.
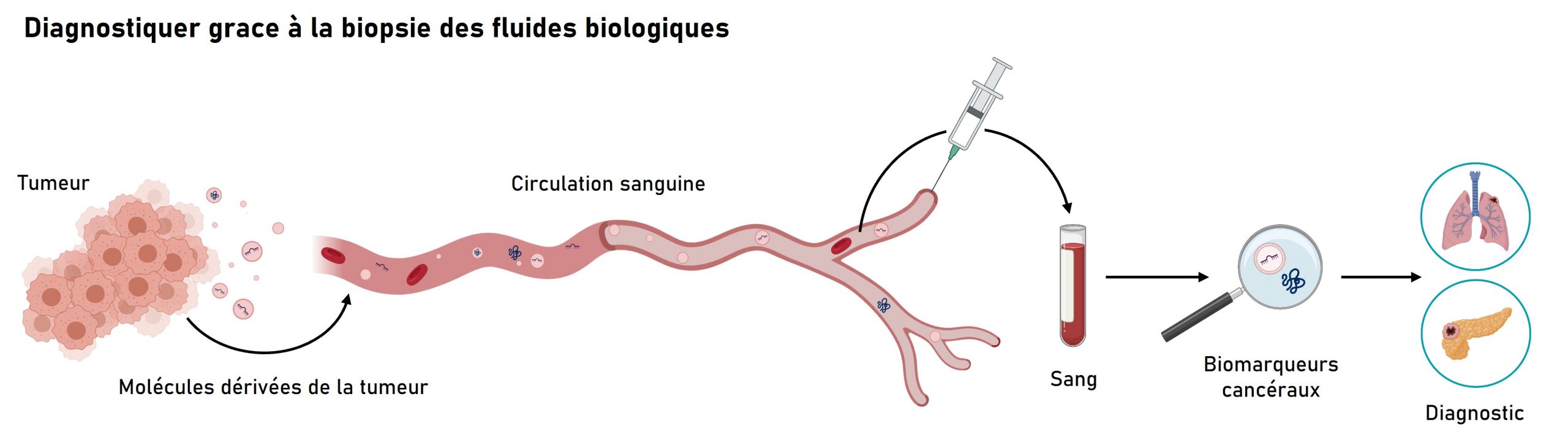
La promesse des ARN exosomaux
L’ARN, un composant clé dans la traduction et la régulation des gènes, est l’un de ces biomarqueurs tumoraux présents des fluides biologiques. Les cellules tumorales sécrètent différentes molécules d’ARN dans la circulation sanguine afin d’influencer les tissus sains de l’organisme. Les micro-ARN (miARN) sont une catégorie de molécules d’ARN qui sont souvent dérégulées encas de cancer. Ils peuvent bloquer la production de protéines spécifiques dans les cellules saines, permettant ainsi à la tumeur d’affecter l’ensemble du corps. Ces miARN sont notamment transportéspar des exosomes, des vésicules extracellulaires qui les protègent de toute dégradation dans le sang.
Au fur et à mesure que la recherche sur les exosomes et les miARN progresse, les scientifiques ont remarqué leur énorme potentiel en tant que marqueurs pour la détection et l’identification rapides des cancers. En effet, les miARN exosomaux présentent des caractéristiques uniques. Ils sont fortement exprimés et stables en dehors des tissus tumoraux d’origine. Ils peuvent également présenter des profils d’expression caractéristiques de la charge tumorale et fournir des informations précieuses sur l’état actuel des tissus tumoraux.
Notre vision
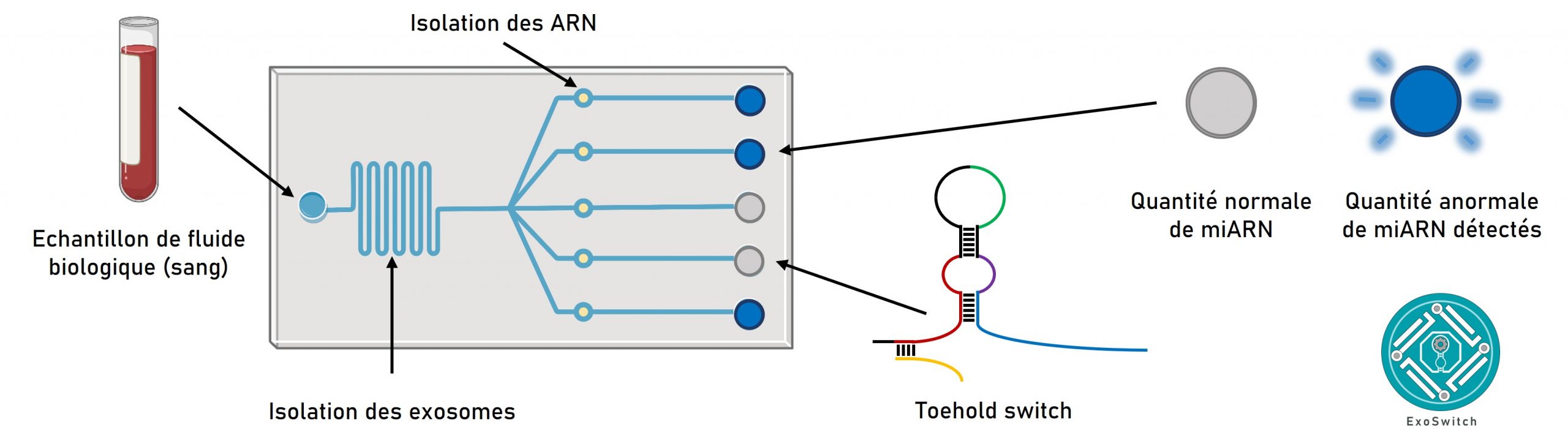
Notre mission est de construire un outil rapide et précis pour la détection des miARN exosomaux dans le sang. Nous commençons par modéliser et synthétiser un ensemble d’outils basé sur la biologie de synthèse : des “toehold switches” -des ARN artificiels qui permettent une détection rapide et spécifique des miARN cibles. Nos objectifs à court terme comprennent :
- Conceptionner une bibliothèque de “toehold switches” pour la détection d’une sélection de miARN liés au cancer.
- Établir une routine de synthèse pour ces “toehold switches”.
- Valider l’utilité des“toehold switches” en affinant leur spécificité et leur sensibilité.
Après avoir validé l’utilité de nos “toehold switches”, nous voulons concevoir un dispositif microfluidique permettant de séparer les miARN exosomaux d’un échantillon de sang et de réaliser la détection de ces derniers grâce aux “toehold switches”. La technologie microfluidique est nécessaire pour construire un prototype correspondant à nos objectifs à long terme :
- Permettre la détection et l’identification de types de cancers basés sur la quantification simultanée des miARN.
- Simplicity of use and implementation by the clinical laboratories around the globe
- Offrir une solution innovante compatible avec une production et une distribution de masse.
Notre projet s’inscrit dans le cadre des objectifs de développement durable (ODD 3 -bonne santé et bien-être) définis par les Nations Unies.

Vous êtes intéressés par notre projet ? Rejoignez-nous !



